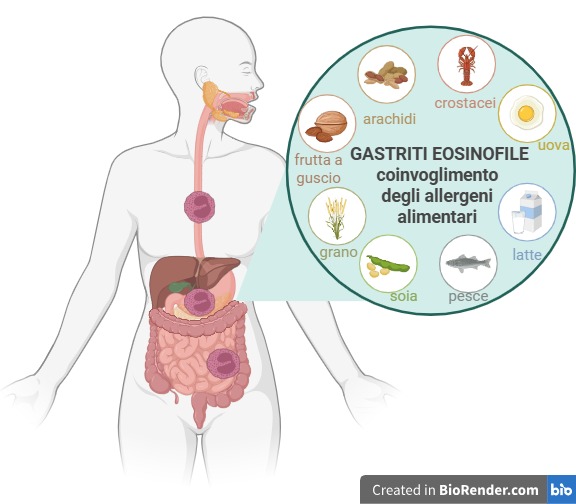
Le gastroenteriti eosinofile fanno parte delle cosiddette malattie gastrointestinali eosinofile (EGIDs), un gruppo di condizioni infiammatorie croniche in cui si verifica un’infiltrazione anomala di eosinofili – cellule del sistema immunitario normalmente coinvolte nelle difese contro i parassiti e nelle reazioni allergiche – all’interno della parete del tratto digestivo. Questo accumulo determina infiammazione persistente e, a lungo andare, danno tissutale.
In base al tratto colpito, si distinguono diverse forme:
- l’esofagite eosinofila (EoE), la più conosciuta e studiata,
- la gastrite eosinofila (EoG),
- la duodenite eosinofila (EoD),
- fino all’interessamento dell’intestino tenue (enterite eosinofila, EoN) o del colon (colite eosinofila, EoC).
I sintomi dipendono dalla sede: difficoltà nella deglutizione e cibo che si blocca in esofago nell’EoE, dolore addominale, nausea, diarrea e perdita di peso nelle forme gastriche o intestinali, fino a sangue nelle feci nella colite eosinofila. Non raramente si osservano malnutrizione e arresto della crescita nei bambini, segno della portata sistemica di queste malattie.
Dal punto di vista immunologico, le EGIDs sono patologie guidate da un’iperattivazione dell’immunità di tipo 2 (Th2): citochine come IL-5, IL-4 e IL-13 stimolano il richiamo e la sopravvivenza degli eosinofili, mentre chemochine come le eotassine ne favoriscono il reclutamento a livello della mucosa. L’epitelio intestinale, danneggiato dall’infiammazione, rilascia ulteriori mediatori (TSLP, IL-33) che amplificano la risposta immunitaria. Gli eosinofili, una volta attivati, liberano proteine tossiche (MBP, ECP) che contribuiscono alla lesione della mucosa, al malassorbimento e in alcuni casi alla fibrosi.
La diagnosi si basa esclusivamente sull’endoscopia con biopsie multiple: non esiste infatti un test del sangue o cutaneo capace di identificare con certezza queste malattie. Per questo motivo il percorso diagnostico è affidato al gastroenterologo, ma la presa in carico richiede un lavoro multidisciplinare: immunologo, allergologo e – soprattutto – nutrizionista.
Diversi sono i farmaci utilizzati in queste patologie:
Corticosteroidi topici o sistemici : Prednisone o budesonide (in formulazioni orali disgreganti o slurry) riducono l’infiammazione. Buoni nell’induzione, ma non sempre sostenibili a lungo termine per effetti collaterali.
Inibitori di pompa protonica (PPI): Utili per ridurre l’acidità ma anche per diminuire l’eosinofilia in un sottogruppo di pazienti.
Biologici in sperimentazione/uso off-label: Dupilumab (anti-IL-4Rα): notati miglioramenti istologici, endoscopici e sintomatologici (trial DEGAS 2025).
Lirentelimab (anti-Siglec-8): potente riduttore degli eosinofili, ma risultati clinici variabili.
Benralizumab (anti-IL-5Rα): efficace sulla deplezione eosinofila, meno sui sintomi.
Nel contesto della multidisciplinarità, la gestione nutrizionale rappresenta infatti uno dei pilastri del trattamento. Non solo perché il cibo è spesso il trigger dell’infiammazione, ma anche perché il paziente con EGID rischia squilibri nutrizionali legati a restrizioni prolungate, selettività alimentare e malassorbimento.
 Malnutrizione e malassorbimento: cosa monitorare
Malnutrizione e malassorbimento: cosa monitorare
L’infiammazione cronica e le restrizioni dietetiche possono portare a carenze nutrizionali significative. I principali aspetti da tenere sotto controllo sono:
- Carenze di ferro e anemia sideropenica: frequente nei pazienti con EoG/EoD, per malassorbimento o perdite occulte.
- Vitamina B12 e folati: a rischio in caso di coinvolgimento gastrico/duodenale, con conseguente anemia megaloblastica.
- Vitamina D e calcio: spesso ridotti, sia per malassorbimento sia per eliminazione dei latticini (tra i trigger più comuni).
- Proteine e albumina: possono ridursi per enteropatia perdente proteine.
- Altri micronutrienti: zinco, magnesio, selenio possono risultare carenti in diete molto restrittive.
Un altro punto fondamentale è il microbiota intestinale: le diete elementali e le restrizioni severe riducono la diversità microbica, con possibili effetti sul metabolismo, sull’immunità e sulla tolleranza alimentare a lungo termine.
Per questo, è fondamentale che ogni percorso dietetico sia seguito da un nutrizionista, con monitoraggio clinico e laboratoristico periodico.
GLI APPROCCI ALIMENTARI IN GASTRITI EOSINOFILE
Dieta elementare (elemental diet)
L’approccio più drastico ed efficace nel breve termine è la dieta elementare. Si tratta di una nutrizione a base di formule esclusivamente composte da amminoacidi liberi, carboidrati semplici, grassi, vitamine e minerali, quindi completamente priva di proteine complesse e potenziali allergeni.
Questa strategia, seguita in genere per 4–6 settimane, porta in una percentuale molto alta di pazienti alla remissione istologica e clinica completa, perché “azzerando” l’esposizione antigenica interrompe l’infiammazione. È quindi un’opzione preziosa nei casi gravi o resistenti ad altre terapie.
Tuttavia, non è un percorso semplice: la palatabilità delle formule è ridotta, i costi sono elevati e la vita sociale viene fortemente condizionata. Per questo spesso si utilizza come terapia d’induzione, seguita poi da una reintroduzione graduale degli alimenti, monitorata con endoscopie successive.
Durata tipica: 4–6 settimane in induzione.
- Vantaggi: remissione completa in alta percentuale di pazienti, azzeramento esposizione agli antigeni alimentari.
- Limiti: palatabilità ridotta, costi elevati, rischio alterazioni microbiota e isolamento sociale.
Esempio di schema (elementare esclusiva):
- Colazione, pranzo, cena e spuntini: formula aminoacidica (in polvere ricostituita o già pronta in brick).
- Idratazione: acqua naturale, tisane non zuccherate, eventuale acqua di cottura di riso/verdure (senza fibre solide).
Dopo la fase di induzione, si passa alla reintroduzione graduale di alimenti, uno alla volta, con endoscopie di controllo.
Diete di eliminazione empiriche
Più sostenibili nel lungo periodo sono le diete di eliminazione. Le principali modalità sono:
- 6-FED (Six Food Elimination Diet): esclusione dei sei alimenti più frequentemente associati a EGIDs – latte, uova, grano, soia, frutta a guscio e pesce/crostacei.
- 4-FED: eliminazione di quattro gruppi (in genere latte, grano, uova e soia).
- 2-FED: eliminazione mirata solo di latte e grano, che risultano i trigger più comuni.
L’approccio oggi più consigliato è quello “step-up”: si parte con un’eliminazione ristretta (es. latte e grano) e, se non si ottiene remissione, si passa a diete più restrittive. Questo evita al paziente esclusioni inutili e riduce il rischio di squilibri nutrizionali.
La durata media dell’eliminazione è di circa 6–8 settimane, seguita da un controllo endoscopico. Se la mucosa risulta guarita, si procede con la reintroduzione graduale degli alimenti esclusi, uno alla volta, sempre con monitoraggio clinico ed endoscopico. In questo modo si identificano i veri alimenti scatenanti, che verranno poi evitati stabilmente.
| Dieta | Alimenti esclusi | Durata tipica | Obiettivo |
| 2-FED | Latte e derivati, grano | 8–12 settimane | Prima linea più sostenibile |
| 4-FED | Latte, grano,
uova, soia |
8–12 settimane | Se la 2-FED non è efficace |
| 6-FED | Latte, grano, uova,
soia, pesce, Frutta a guscio |
6–8 settimane | Opzione più restrittiva se necessario |
Tabella pratica – 6-FED
| Gruppo escluso | Alimenti da evitare | Alternative consentite |
| Latte e derivati | latte vaccino, formaggi, yogurt, burro | bevande vegetali fortificate (riso, avena, mandorla se tollerata), olio EVO, olio di cocco |
| Grano | pane, pasta, couscous, prodotti da forno | riso, mais, quinoa, grano saraceno, patate |
| Uova | uova intere, prodotti da forno con uova | prodotti “egg-free”, legumi come legante, semi di lino |
| Soia | salsa di soia, tofu, latte di soia | altri legumi (ceci, lenticchie), salsa tamari senza soia |
| Frutta a guscio | nocciole, mandorle, pistacchi, arachidi | semi (zucca, girasole), burro di semi |
| Pesce e crostacei | pesce fresco, molluschi, crostacei | carne bianca, legumi |